4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-905KJ·mol-1
来源:学生作业帮 编辑:神马作文网作业帮 分类:化学作业 时间:2024/10/05 03:21:15
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-905KJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-905KJ·mol-1
若将此化学方程式中各无知的系数均乘以2,应如何书写化学方程式?
答案是8NH3(g)+10O2(g)=8NO(g)+12H2O(g) ΔH=-1810KJ·mol-1
还是8NH3(g)+10O2(g)=8NO(g)+12H2O(g) ΔH=-905KJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-905KJ·mol-1
若将此化学方程式中各无知的系数均乘以2,应如何书写化学方程式?
答案是8NH3(g)+10O2(g)=8NO(g)+12H2O(g) ΔH=-1810KJ·mol-1
还是8NH3(g)+10O2(g)=8NO(g)+12H2O(g) ΔH=-905KJ·mol-1
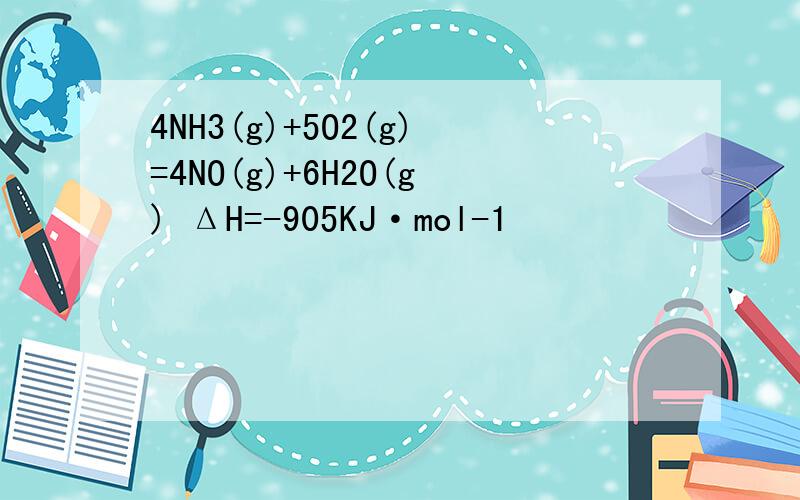
8NH3(g)+10O2(g)=8NO(g)+12H2O(g) ΔH=-1810KJ·mol-1
方程式系数变为原来的二倍,反应的热之自然也是二倍
方程式系数变为原来的二倍,反应的热之自然也是二倍
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-905KJ·mol-1
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= - 1025kJ/mol该反应是一个可逆反应.
判断题:已知 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔrHmθ=-1170 kJ·mol-1
工业制硝酸的主要反应是:4NH3(g)+5O2(g)= 4NO(g)+6H2O (g);△H = -1025 kJ
解释下述热化学方程式表示的含义:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905Kj*mol(
4nh3(g)+5o2(g) 4no(g)+6h2o(g) Δh
4NH3(g)+5O2(g)==4NO(g)+6H2O(g),请问1molNH3转移几mol电子
已知热化学方程式:H2O(g)=H2(g) O2(g) △H= 241.8kJ·mol-1; H2(g) O2(g)=H
已知2H2(g)+O2(g)=2H2O(1)^H=_571.6kj·mol·-1CO(g)+1/2O2(g)==CO2(
高二化学2H2(g)+O2(g)=2H2O(1) △H=571、6kj、mol-1次方 C3H8(g)+5O2(g)=3
H2(g)+1/2O2(g)==H2O(g) △H=+242KJ/mol , 2H2(g)+O2(g)==2H2O(g)
已知4NH3(g)+5O2(g)=4NO(g)+6H2O(g),若反应速率分别是v(NH3)、v(O2)、v(NO)、v