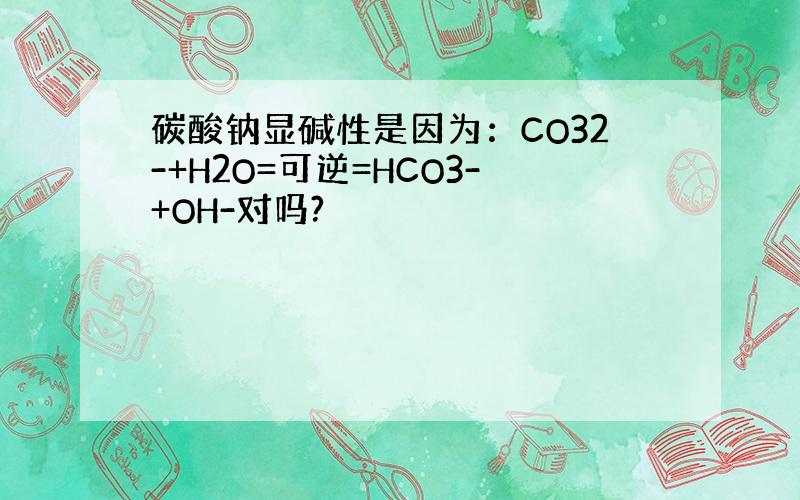
碳酸钠显碱性是因为:CO32-+H2O=可逆=HCO3-+OH-对吗?
碳酸钠显碱性是因为:CO32-+H2O=可逆=HCO3-+OH-对吗?
HCO3-+OH-=H2O+CO32- 是电离方程么
CO32-+H+=HCO3-和CO32-+H2O=HCO3-+OH-有什么不同
HCO3-+OH-==CO32-+H2O的对应化学方程式
H2O+AlO2- +HCO3 - = Al(OH)3↓+CO32-
alo2-+hco3-+h2o=al(oh)3+co32-为什么是强酸制弱酸?
CO32- + H2O== HCO3-+ OH- HCO3-,如果HCO3-与水中弱电离的H-生成碳酸,那碳酸又是酸性的
碳酸钠溶液与盐酸反应:CO32–+H+=HCO3- 或CO32–+2H+=CO2↑+H2O 这是为什么呢?第一个是怎么回
离子方程式:CO32- +CO2+H2O=HCO3-
HCO3- + ALO2- + H2O===CO32- + AL(OH)3 可见:ALO2- 》CO32- 故可判断酸性
在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O==HCO3-+OH-
na2co3中和浓酸,老师上课说起co32-+H2O=hco3- +oh-,不懂.