已知:2CH3OH(g) CH3OCH3(g) + H2O(g),ΔH=-25 kJ/mol
来源:学生作业帮 编辑:神马作文网作业帮 分类:化学作业 时间:2024/09/23 09:23:34
已知:2CH3OH(g) CH3OCH3(g) + H2O(g),ΔH=-25 kJ/mol
此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
物质 CH3OH CH3OCH3 H2O
c/(mol·L-1) 0.8 1.24 1.24
1 .平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率该如何变化
2.平衡时,反应混合物的总能量该如何变化
请您帮我尽量详细分析
此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
物质 CH3OH CH3OCH3 H2O
c/(mol·L-1) 0.8 1.24 1.24
1 .平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率该如何变化
2.平衡时,反应混合物的总能量该如何变化
请您帮我尽量详细分析
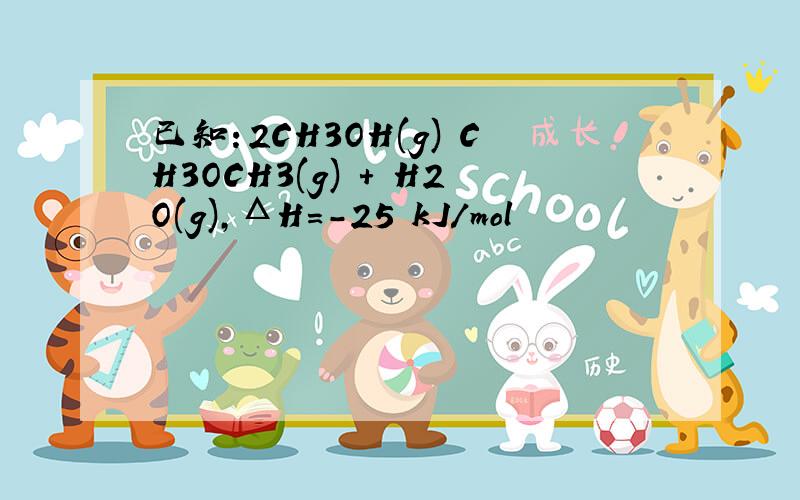
1.再加入与起始量等的CH3OH,先假设这些CH3OH是放入旁边容器中,那麼此时新平衡和原平衡是等效的.然後把中间隔板拿走,混合之後平衡不移动.最後把体积压缩回原来大小.由於压缩体积平衡不移动,因此最终还是等效平衡,所以转化率不变.
2.因为是放热反应,所以能量要降低.
再问: 再请问一下 混合物的总能量的减少量该怎么算
再答: 这个算不出来的 因为你没给反应热也没给物质的量也没给转化率
再问: 已知 : 反应热ΔH=-25 kJ/mol 由这道题算出的: CH3OH平衡浓度为1.6mol/l 起始浓度为3.28mol/l
再答: 3.28到1.6mol,相当於只有1.68mol的CH3OH反应 2CH3OH(g) CH3OCH3(g) + H2O(g)ΔH=-25 kJ/mol 2mol反应放热25kJ 那麼1.68mol放热就自己去算了
2.因为是放热反应,所以能量要降低.
再问: 再请问一下 混合物的总能量的减少量该怎么算
再答: 这个算不出来的 因为你没给反应热也没给物质的量也没给转化率
再问: 已知 : 反应热ΔH=-25 kJ/mol 由这道题算出的: CH3OH平衡浓度为1.6mol/l 起始浓度为3.28mol/l
再答: 3.28到1.6mol,相当於只有1.68mol的CH3OH反应 2CH3OH(g) CH3OCH3(g) + H2O(g)ΔH=-25 kJ/mol 2mol反应放热25kJ 那麼1.68mol放热就自己去算了
已知:2CH3OH(g) CH3OCH3(g) + H2O(g),ΔH=-25 kJ/mol
CH3OCH3(g)+H2O(g) (可逆符号)2CH3OH(g)△H=+37kJ/mol,现有三个相同的2L恒容绝热(
(2014•淄博三模)己知:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1.某温度下
已知反应②2CH3OH(g) CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 .
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-Q1 kJ/mol,2H2(g)+O2(g)==
反应CO2(g)+3H2(g)==CH3OH(g)+H2O(g),△H=-a KJ/mol.在1L密闭容器中充入1mol
已知2H2(g)+O2(g)=2H2O(g)△H=-484kj/mol 2H2(g)+O2(g)=2H2O(l)△H=-
H2(g) + 1/2O2(g) = H2O(g) ;△H=-241.8 KJ/mol 2H2(g) + O2(g) =
已知下列两个热化学方程:2H2(g) + O2(g) = 2H2O(l) △H=-571.6 kJ/mol
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kj/mol 2h2(g)+O2(g)=2H2O(g)
已知(1)2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ.mol-1
5、已知下列两个热化学方程式:2H2(g)+O2(g)=2H2O(l) △H = -571.6 kJ/mol拜托了各位