HCO3- + H20 ====H2CO3 + OH-
来源:学生作业帮 编辑:神马作文网作业帮 分类:化学作业 时间:2024/09/28 05:32:02
HCO3- + H20 ====H2CO3 + OH-
比较水解程度大还是电解程度大 这里的电解程度是指 HCO3- 的电解还是指产生的H2CO3的电解
假如得出 水解大于电离 则电离的式子是不是可以省略不写?
比较水解程度大还是电解程度大 这里的电解程度是指 HCO3- 的电解还是指产生的H2CO3的电解
假如得出 水解大于电离 则电离的式子是不是可以省略不写?
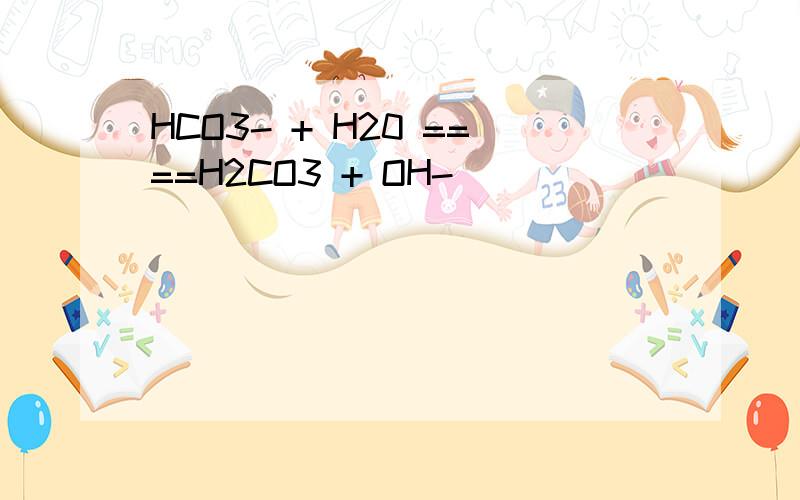
以碳酸氢钠为例:
HCO3-离子在溶液中既可发生电离又可发生水解,只是电离和水解程度不同,其进行程度都较小.
这里的电离是指HCO3-的电离.
其水解程度大于电离程度,但也不能忽略掉电离的影响,判断一些离子或分子浓度的大小的时候还是要考虑进去的!
再问: CH3COO- + H20 ==== CH3COOH + OH- 那这里比较电离程度和水解程度 电离程度怎么看? CH3COO- 没办法像HCO3- 那样再次电离
再答: 这里只有水解,没有电离,不需要再比较电离程度和水解程度了!
HCO3-离子在溶液中既可发生电离又可发生水解,只是电离和水解程度不同,其进行程度都较小.
这里的电离是指HCO3-的电离.
其水解程度大于电离程度,但也不能忽略掉电离的影响,判断一些离子或分子浓度的大小的时候还是要考虑进去的!
再问: CH3COO- + H20 ==== CH3COOH + OH- 那这里比较电离程度和水解程度 电离程度怎么看? CH3COO- 没办法像HCO3- 那样再次电离
再答: 这里只有水解,没有电离,不需要再比较电离程度和水解程度了!
HCO3-+H2O==H2CO3+OH
CO3 2- +H20=HCO3-+OH-反应属于
已知KHCO3溶液呈碱性,对于平衡:HCO3-+H2O= H2CO3 + OH-,欲使溶液
在0.1mol.l-的Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)对吗?为什么
0.1mol/LNaHCO3溶液中:c(Na+)+c(OH-)=c(HCO3)+2c(CO3 2-)+c(H2CO3)
二氧化碳水溶液中存在如下平衡:H2CO3=H++HCO3-和HCO3-=H++CO32-
1 H2CO3+KOH 为什么不可以用 H+ + OH- =H20表示?2 防止铁制品生锈不可以局部镀铜?
1:Na2CO3+H20=NaOH+NaHCO3 2:NaHCO3+H20=NaOH+H2CO3 反应1比二生成NAOH
碳酸氢钠酸碱性的疑问虽然碳酸氢钠的水解反应 HCO3-+H2O==(可逆)H2CO3+OH-产生了氢氧根离子,但碳酸氢根
下列平衡体系属於电离平衡的是 A:hco3- +h2o=h2co3+oh- B:hs-+h2o=h3o+ + s2- C
盐类水解的实质是生成的弱电解质破坏了水的电离平衡 例如:HCO3- +H2O可逆=H2CO3+OH-
等浓度的碳酸钠和碳酸氢钠溶液混合后的溶液中:2c(OH-)+c(CO32-)=c(HCO3- )+3c(H2CO3)+2